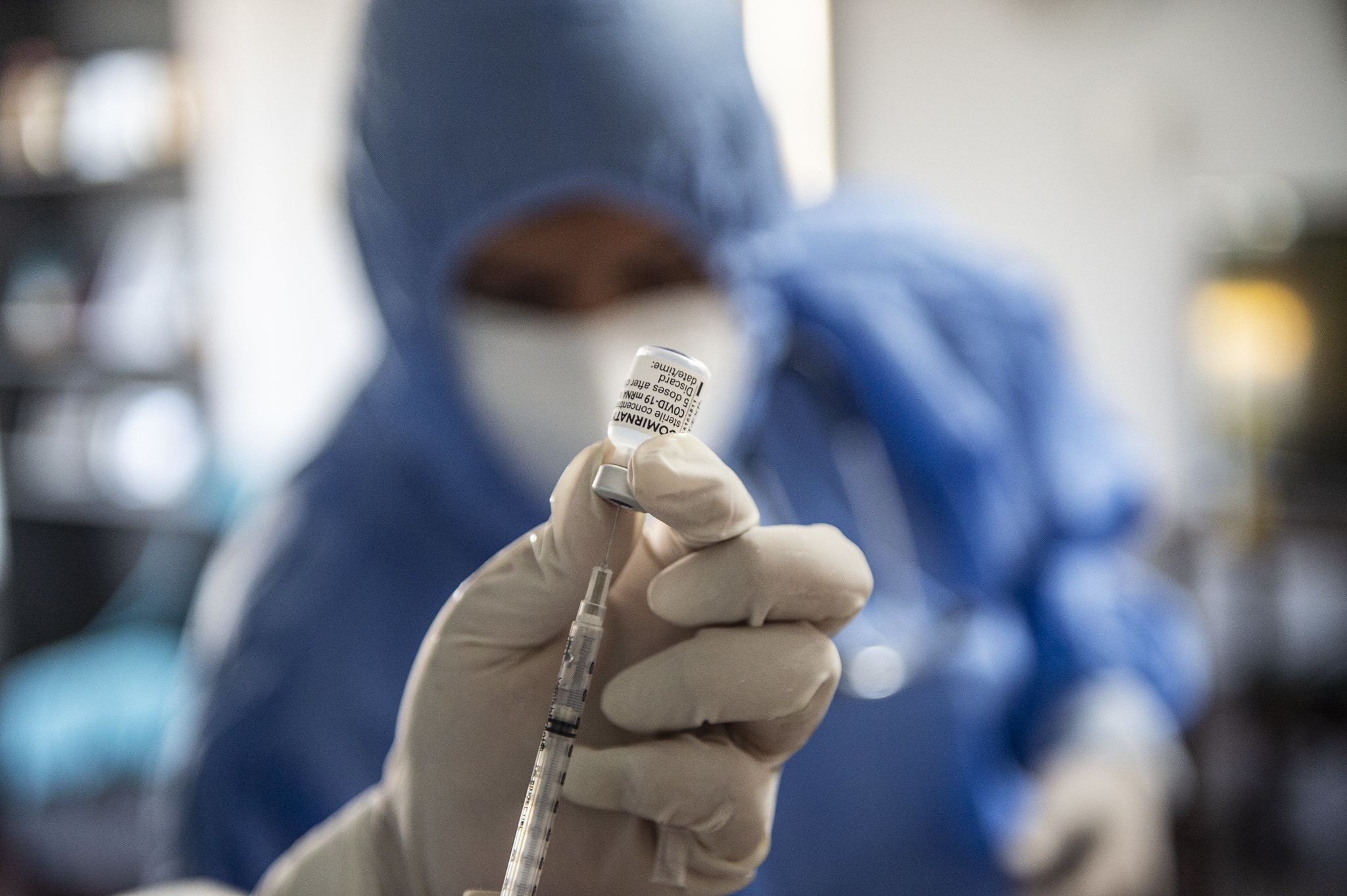
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta última sexta-feira (16) a ampliação de uso da vacina da Pfizer para bebês a partir de 6 meses contra a covid-19. A decisão permite o início do uso da substância para este público até 4 anos de idade. A partir de agora, cabe ao Ministério da Saúde a incorporação da vacina no plano de imunização, com o estabelecimento do calendário para as faixas etárias específicas.
Segundo a Anvisa, a avaliação teve início em 1º de agosto e contou com análise criteriosa da área técnica com a celeridade solicitada. Para a avaliação da ampliação da faixa etária, o órgão contou com a consulta e o acompanhamento de um grupo de especialistas de sociedades médicas, que teve acesso aos dados dos estudos e resultados apresentados pelo laboratório norte-americano.
Participaram da análise a Associação Brasileira de Saúde Coletiva (Abrasco), a Sociedade Brasileira de Pneumologia e Tisiologia (SBPT), a Sociedade Brasileira de Infectologia (SBI), a Sociedade Brasileira de Imunologia (SBI), além da Sociedade Brasileira de Pediatria (SBP). A vacina da Pfizer está registrada no Brasil desde o dia 23 de fevereiro de 2021. Em 16 de dezembro de 2021, a Anvisa já havia autorizado a indicação para a faixa etária de 5 a 11 anos.
A vacina para crianças entre 6 meses e 4 anos de idade terá dosagem e composição diferentes daquelas utilizadas para as faixas etárias previamente aprovadas. A inoculação deve ser feita em três doses de 0,2 ml (equivalente a 3 microgramas). As duas doses iniciais devem ser administradas com três semanas de intervalo, seguidas por uma terceira dose administrada pelo menos oito semanas após a segunda dose.
Além disso, a tampa do frasco virá na cor vinho, para facilitar a identificação pelas equipes de vacinação e, também, pelos pais, mães e cuidadores que levarão as crianças para serem picadas. O uso de diferentes cores de tampa é uma estratégia para evitar erros de administração, já que o produto requer diferentes dosagens para diferentes faixas etárias.|