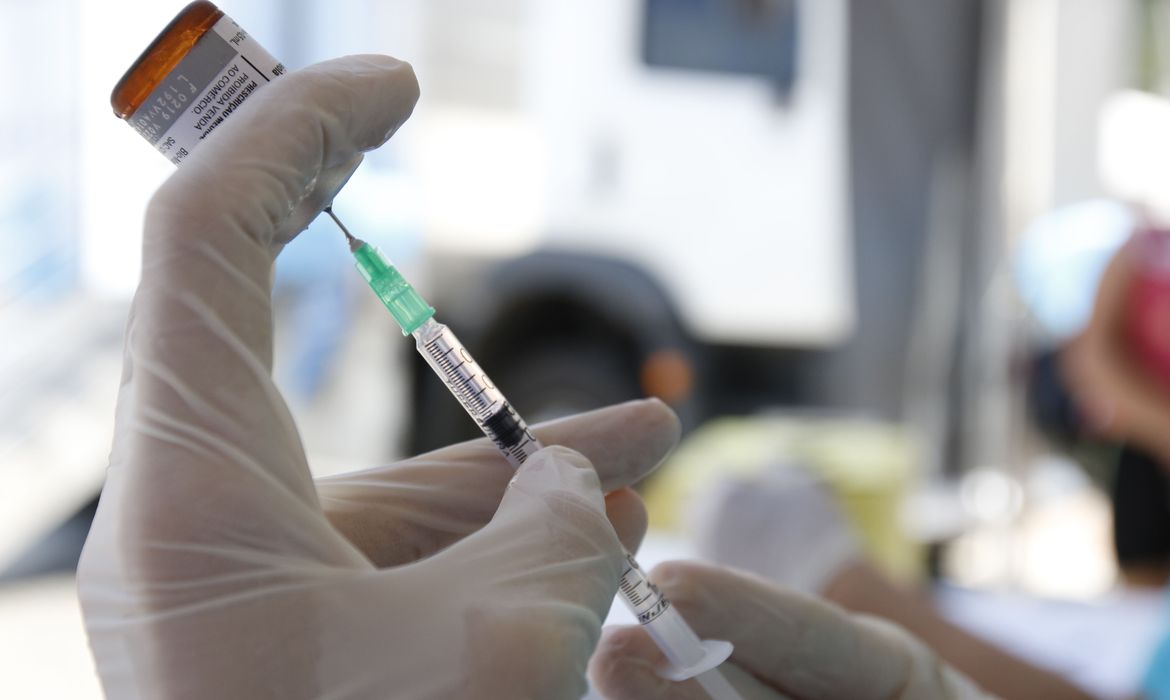
Pouco mais de um mês após início da vacinação no Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) considera que os eventos adversos mais frequentes relacionados às vacinas contra a covid-19 não são graves e estão dentro do esperado. Segundo a agência reguladora, não há até o momento dados que indiquem mudanças na avaliação da segurança dos imunizantes.
Em entrevista, a gerente-geral de Monitoramento de Produtos Sujeitos à Vigilância Sanitária da Anvisa, Suzie Marie Teixeira Gomes, exemplificou alguns desses eventos. “Dor de cabeça, febre, aquela sensação de gripe que muita gente relata pós-vacinação são os eventos mais frequentes. Então, não são eventos graves, são eventos esperados”, declarou. “São efeitos que acontecem com outras vacinas e outros medicamentos também”, acrescentou.
A gerente ponderou, no entanto, que ainda é muito cedo para avaliar os dados sobre o uso das vacinas no Brasil, pelo fato de o número de vacinados no país ainda ser pequeno se comparado a outras vacinas que integram o Programa Nacional de Imunizações (PNI).
“Não existe, até o momento, nenhum sinal de segurança importante para que se desencadeie um processo regulatório ou uma ação regulatória. Toda essa avaliação vem sendo feita desde a primeira agulhada que foi administrada na primeira dose. Ainda é muito cedo porque o número de pessoas vacinadas ainda é muito pequeno em relação a outras vacinas. Então, as suspeitas que são notificadas, mais as informações adicionais de outras autoridades regulatórias, com a base de dados da Organização Mundial da Saúde, não mostraram para a gente nenhuma alteração no perfil de segurança da vacina. Isso é um ponto muito positivo”, disse Suzie.
A Anvisa deve receber nos próximos dias relatórios de benefício-risco dos fabricantes das vacinas CoronaVac e Oxford/AstraZeneca, com dados sobre o primeiro mês da aplicação no país. Esses documentos vão auxiliar o monitoramento da segurança dos imunizantes.
As informações são da Agência Brasil.